近日,Trends in Biotechnology在线发表了welcome皇冠地址登录入口未来食品科学中心和welcome皇冠地址登录入口陈坚院士团队的综述Recent advances in the microbial synthesisof hemoglobin。赵鑫锐副研究员为第一作者,周景文教授为通讯作者,论文作者还包括陈坚教授和堵国成教授。
血红蛋白是一类存在于原核和真核细胞中的以血红素为辅基的含铁金属蛋白,在生物体内具有运输和储存氧、调节胞内pH值、调控生理代谢等诸多重要功能。近年来,血红蛋白已经被应用于急诊医学(作为无细胞氧载体)、医疗保健(作为铁补给剂)、食品加工(食品级着色和调味剂)等领域。但血红蛋白的获取依然需要依靠从血液或植物组织中提取,提取法不仅费时低效、并且所用化学试剂还易造成环境污染。因此,以微生物细胞工厂为平台来合成不同来源的血红蛋白已经成为近年来的研究热点。
在NCBI的GeneBank数据库中已有超过141110条的血红蛋白基因编码序列,在EMBL蛋白数据库中已有超过84424条的血红蛋白氨基酸序列,在PDB蛋白晶体数据库中也已经有725条血红蛋白的三维结构数据,但现阶段其中只有15种不同来源(人、大豆、鳄鱼等)的血红蛋白可由9种有限的微生物(大肠杆菌、酿酒酵母、枯草芽孢杆菌等)合成。根据对现有血红蛋白氨基酸序列进行系统发育树分析,发现不同来源的血红蛋白及其亚基分为几类:动物来源血红蛋白α亚基、β亚基以及其他类型亚基,植物来源单亚基血红蛋白、微生物来源血红蛋白(图1)。因此,可以综合应用目前越来越成熟的代谢工程和合成生物学策略,开发出有效且稳定的血红蛋白微生物合成方法,来满足对人、大豆、透明颤菌等不同物种血红蛋白的大规模应用的需求。
血红素是血红蛋白执行其生理功能所必需的辅基,要想高效合成血红蛋白首先需要提高胞内血红素的供给水平。在自然界中血红素的合成主要通过C4和C5两种途径(图2),通过强化C4途径并补加甘氨酸和琥珀酸作为底物或强化抗反馈抑制的C5途径都可以增加胞内血红素前体5-氨基酮戊酸(ALA)的含量。在此基础上继续强化并模块化改造血红素合成的下游途径,可在大肠杆菌中不添加底物的情况下实现115.5±2.3mg/L血红素的合成。此外,由于胞内过高含量的血红素会显著抑制菌体的生长,利用血红素转运蛋白可以实现超过60%血红素的分泌合成,以减轻血红素对细胞的毒性作用。
在提高血红素供给水平的基础上,利用大肠杆菌、酵母等微生物宿主合成不同来源血红蛋白已获得成功。由于代谢改造成熟和培养成本低廉,目前超过70%的血红蛋白均由大肠杆菌合成。首先为了增强大肠杆菌中血红蛋白的可溶性,密码子优化、启动子和载体的适配组合、以及蛋白促溶标签均已被成功应用来避免包涵体的形成;其次为了增强动物来源血红蛋白α亚基的表达量,α亚基编码基因的串联表达和稳定辅因子AHSP的共表达也已被用于提高α亚基的稳定型;此外由于大肠杆菌宿主中血红素的合成和运输能力较弱,可以通过引入志贺假单胞菌的血红素转运系统并在胞外添加高浓度的血红素,以增加细胞内血红素水平(图3)。在初步获得血红蛋白的基础上,还可以进一步通过:将人源血红蛋白α亚基和牛源血红蛋白β亚基相结合,开发出一种自聚合的人牛杂源血红蛋白(180-500kDa聚合物)来延长商业化无细胞氧载体产品在血液中的半衰期;在宿主中共表达甲硫氨酸氨基肽酶以加速血红蛋白N末端蛋氨酸残基的正确切除;优化诱导剂浓度、诱导温度等发酵条件来提高血红蛋白的产量。
除大肠杆菌之外,酿酒酵母、毕赤酵母等酵母菌株也是合成血红蛋白的高效平台。但在前期研究中,酿酒酵母合成血红蛋白的产量较低,近几年通过优化血红蛋白α和β亚基之间表达水平的比率、强化血红素合成途径、敲除转录因子Hap1p改造氧气传感途径(图3),人源血红蛋白的最高含量可以达到细胞中总可溶性蛋白的7%。毕赤酵母是目前生产商业化大豆血红蛋白的高效宿主,所得大豆血红蛋白可添加到新型人造肉产品中来模拟真肉的肉色和风味。Impossible Foods公司开发的可以商业化合成大豆血红蛋白的毕赤酵母菌株,已经获得了FDA的许可并在多个国家申请了专利。在该菌株中血红素合成所需的八种酶被分为三个模块,并分别用甲醇诱导的AOX1启动子进行了强化表达;此外两个拷贝的大豆血红蛋白的基因和转录激活因子Mxr1p也被整合到基因组中;最后,通过优化高密度发酵条件,实现了大豆血红蛋白的大规模工业生产(图3)。
目前利用微生物来合成血红蛋白虽然已经获得了成功,但大部分血红蛋白的产量还较低,这对在生产中应用重组血红蛋白提出了重大挑战。在未来的研究中可以采用新的策略来进行强化菌株的合成能力(图4):首先可以通过深度学习的方法发现编码未知的具有特殊功能或特性的血红蛋白基因,例如具有高温不易变色特性的三叶草血红蛋白等;其次应继续寻找血红素合成途径中的限速步骤,并应用蛋白质支架等策略解除这些步骤之间的空间隔离;再次应抑制胞内血红素合成途径中的副产物和血红素加氧酶对血红素的降解;最后由于血红素对细胞有毒性作用,并且血红素合成途径中酶的过度表达会增加宿主的代谢负担,因此应用血红素感应器来实现血红素合成和血红蛋白表达之间的代谢平衡是突破血红蛋白合成瓶颈的关键。
本综述得到了国家重点研发计划项目(2019YFA0906400)、国家自然科学基金(31900067)、“轻工技术与工程1”国家一流学科项目(LITE2018-08)的资助,以“Recentadvances in the microbial synthesis of hemoglobin”为题发表在期刊Trendsin Biotechnology上(Trendsin Biotechnology, 2021, 39(3), 286-297, https://www.sciencedirect.com/science/article/abs/pii/S0167779920302262)。
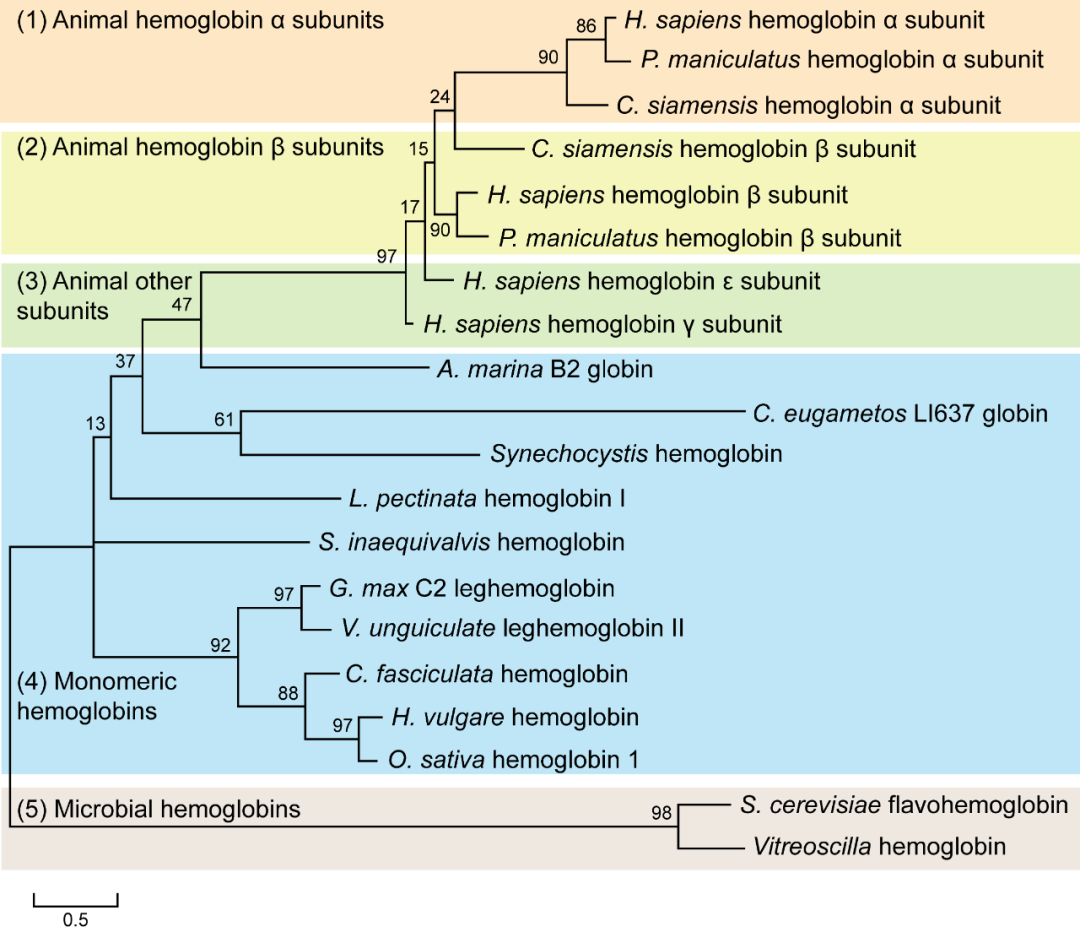
图1 血红蛋白的系统发育树分析
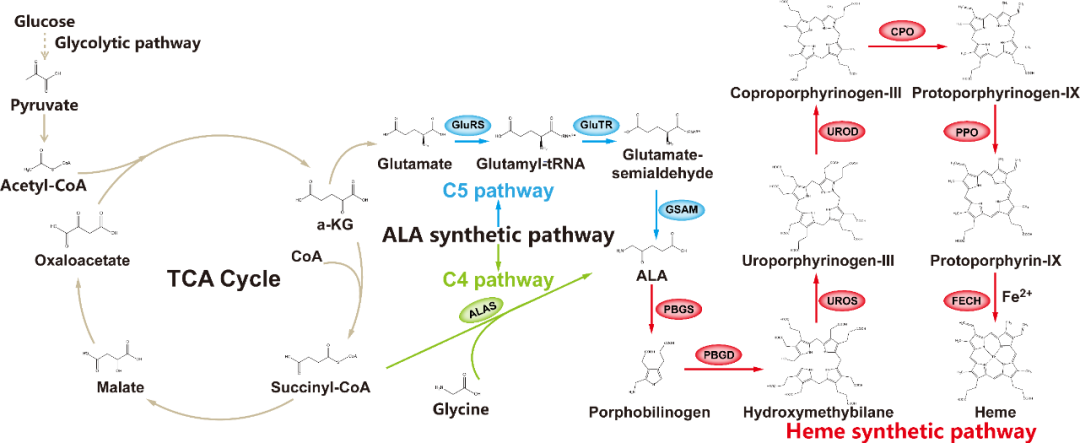
图2 血红素及其前体合成途径
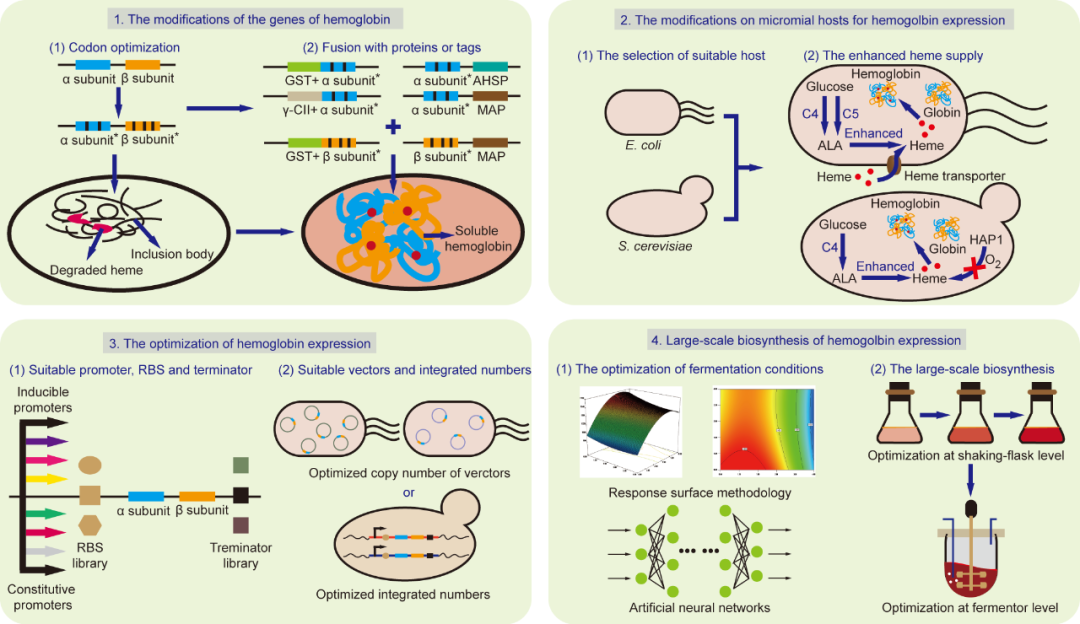
图3 用于增强微生物合成血红蛋白的策略
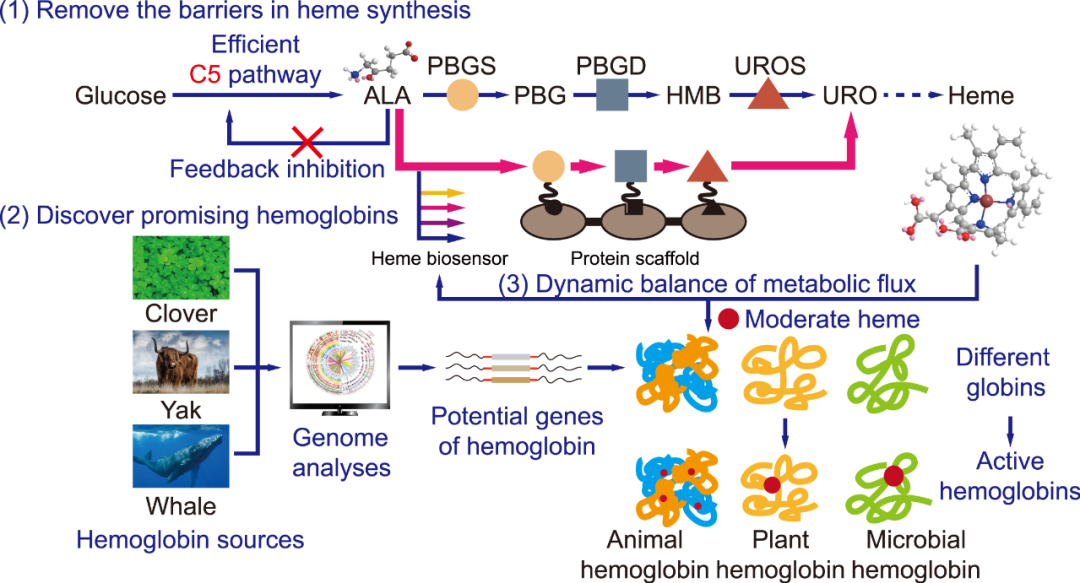
图4 未来可用于进一步提高微生物合成血红蛋白能力的策略
